钛镍合金因具有良好的性能成为心血管支架的首选材料,但常用的激光切割制备的支架表面粗糙,植入人体后易导致腐蚀和溶血,因此需要进行表面处理。电解抛光因具有抛光效率高、效果好等优点常作为钛镍合金支架的最后一道处理工序。 目前常用的抛光液体系为酸⁃醇体系[1⁃3],如硝酸⁃正丁醇[4]、硫酸⁃甲醇[5]等,该体系抛光效率高、效果好,但腐蚀性强、危险系数高,在基础抛光液中加入如氟化铵[6]、柠檬酸[7]、乳酸[8]、三乙醇胺[9]等添加剂能进一步优化抛光效果。
针对钛镍丝材粗糙表面引起的腐蚀、溶血问题,本文以酸⁃醇抛光液为基础抛光液、有机酸和醇为添加剂,研究抛光液成分对钛镍合金丝材抛光效果的影响,以获得适宜的抛光液成分,提高钛镍丝材的表面质量、抗腐蚀性和生物相容性。
1、 实验原料与方法
1.1 实验原料与设备
实验原料为经低温热处理和初步机械抛光的49.2Ti50.8Ni合金丝材,规格为Ф0.5mm×10 mm。 实验所用化学试剂包括高氯酸、柠檬酸、甲醇、甘油、磷酸、 无水乙醇等, 均为分析纯。 主要实验仪器为IT6833 型直流稳压电源、DS⁃101S 集热式恒温加热磁力搅拌器、烧杯、超声波清洗仪、玻璃棒等。
1.2 电解抛光
丝材预处理: 将丝材试样浸没在恒温 50 ℃ 的62%磷酸[10]溶液中,搅拌条件下浸泡 30min,取出后用无水乙醇超声清洗 10min,干燥后装入密封袋中。
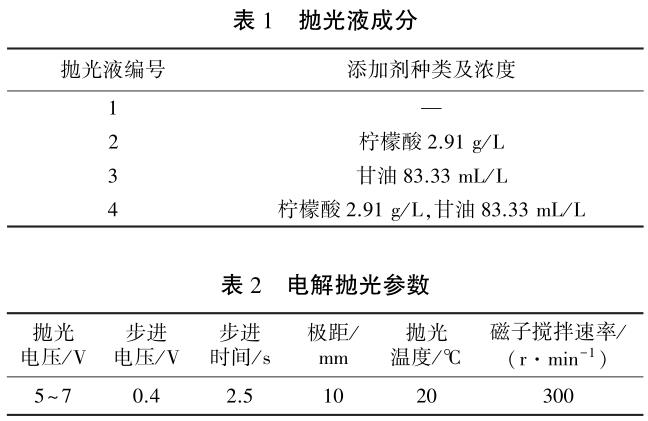
电解抛光:以预处理后的丝材试样为阳极、铂片(10 mm × 10 mm)为阴极,阴极和阳极均完全浸没在抛光 液 中, 在 IT6833 型 直 流 稳 压 电 源 ( 通 过 软 件PV6800 调控电压参数)上进行电解抛光,抛光液基础成分为:12 mL 高氯酸+108 mL 甲醇。 各抛光液添加剂种类及浓度与电解抛光参数分别如表 1 与表 2 所示。
1.3 微观形貌表征
采用 MIRA3 LMH 扫描电子显微镜表征试样表面形貌;通过 Dimension Icon 原子力显微镜评价试样表面粗糙度。
1.4 抗腐蚀性能
采用 IM6ex 型电化学工作站,测试试样极化曲线:参比电极为饱和甘汞电极,阴极为铂电极,测试介质为37 ℃磷酸盐缓冲溶液(PBS),电压测试范围-0.4~0.3 V,扫描速率为 1 mV/ s。
采用 SPECTRO BLUE SOP 全谱直读等离子体发射光谱仪测定 PBS 中镍离子浓度:将试样浸泡在 PBS中,恒温 37 ℃,每 12 h 更换一次 PBS 以模拟人体中体液的流动,分别测试第 1、3、7 和 14 d 的 PBS 中镍离子浓度。
1.5 血液相容性能
溶血率测试:离心管中加入 10 mL 生理盐水作为阳性对照组,离心管中 10 mL 去离子水作为阴性对照组,将试样浸泡在 10 mL 生理盐水中、37 ℃ 水浴保温30 min 作为实验组,然后在阳性对照组、阴性对照组和实验组中分别加入 0.2 mL 稀释抗凝兔血(抗凝兔血与生理盐水体积比 4 ∶5),轻轻摇晃均匀后在 37 ℃ 下保温1 h,以离心速度 2 000 r/ min 对溶液离心 5 min,取上层清液在 550 nm 处测试吸光度值。
式中 OD实验为实验组吸光值;OD阳性为阳性对照组吸光值;OD阴性为阴性对照组吸光值。

血小板黏附实验:将样品放置在 12 孔板中,取新鲜抗凝兔血加入离心管中,以离心速度 1 200 r/ min 离心 10 min,取上层富血小板血浆浸没孔板中的样品,37 ℃恒温培育 2 h 后取出孔板,用 PBS 漂洗两次,以去除未黏附的血小板,再加入戊二醛固定 12 h,经过30%、50%、70%、80%、90%和 100%酒精梯度脱水和喷金后,在扫描电镜下观察血小板黏附情况。
2、结果与讨论
2.1 添加剂对抛光过程的影响
为选择合适的抛光电压,以抛光液 1 为例,探究了电解抛光钛镍丝材过程中的电压⁃电流关系,如图 1(a)所示。 图中 BC 段电流随着抛光电压升高达到近似平台值,此阶段为钝化抛光阶段;CD 段电流随电压升高急剧升高,为过钝化出光阶段;AB 段处于活化溶解阶段,粗糙度有初步改善;抛光电压高于 D 点后处于过钝化阶段,电压过大,阳极迅速溶解,气体剧烈逸出导致抛光液沸腾,抛光效果差。 为了获得更好的抛光效果,结合钝化整平和过钝化出光 2 个阶段,在 BCD 段电压中选择一段连续变化电压作为抛光电压,经前期预实验确定抛光电压范围为 5~7 V。
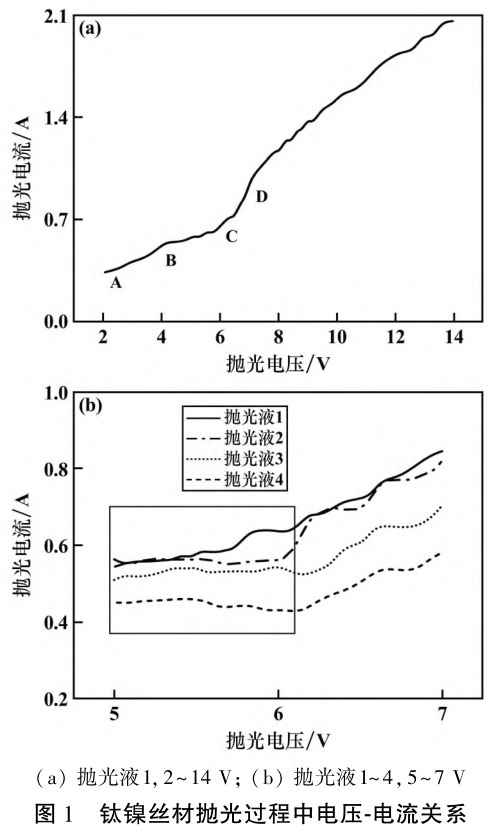
图 1(b)为抛光电压 5~7 V 时钛镍丝材在不同抛光液中的抛光电压⁃电流关系。 可以发现,添加柠檬酸和甘油使电流平台值更明显,这是因为抛光液 2 中柠檬酸与阳极溶解出的 Ni2+形成可溶性络合物,主要以NiCit-形式存在[11],随着抛光过程的进行,络合物逐渐在阳极积累,形成一层液膜,在粗糙的样品表面凸处液膜薄、电阻小,因此凸处溶解电流大,溶解出的阳离子更易扩散,溶解速度大于凹处,表面得到整平;抛光液 3中甘油是表面活性剂且黏度大,溶解的阳离子更容易在阳极积累形成液膜;与单独添加柠檬酸或甘油相比,两者同时添加的抛光液 4 的缓蚀效果更好。
2.2 表面形貌
图 2 为电解抛光前后钛镍丝材表面形貌。 抛光前样品经初步机械抛光后留下的划痕明显且深浅、分布不均匀,表面粗糙。 经抛光液 1 抛光后,样品表面质量已经得到很大改善,尤其划痕数量明显减少,表面较为均匀,但依然存在较深的凹坑。 经过抛光液 2、3 抛光,样品表面明显更均匀平整,划痕去除,柠檬酸和甘油的添加使抛光效果得到提升,但表面有少量蚀坑,这可能是因为抛光过程中丝材表面局部电流过大,导致腐蚀严重形成蚀坑。经抛光液 4 抛光后样品表面平整光滑,几乎观察不到蚀坑,抛光效果好。

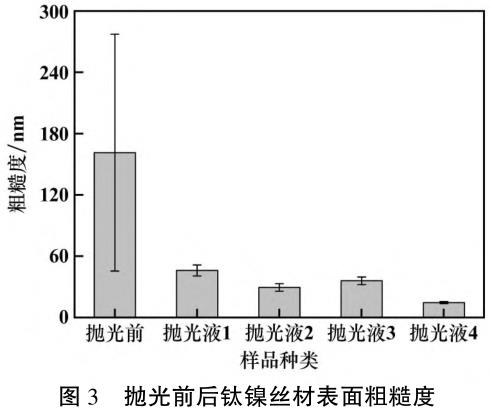
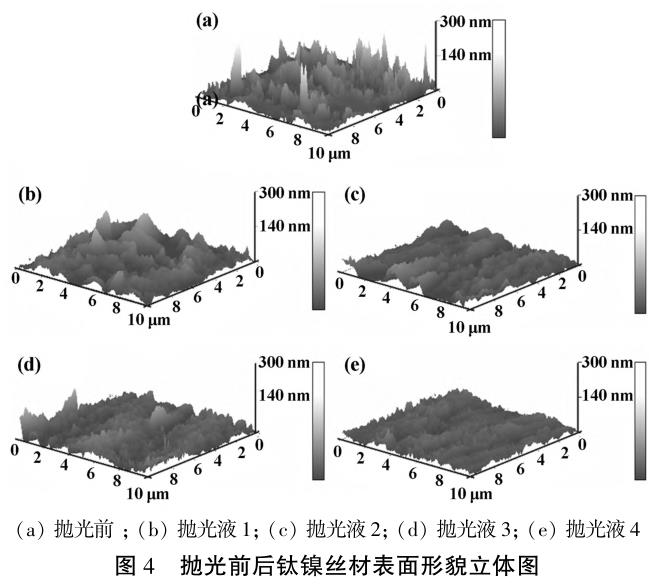
粗糙度可以量化表面平整程度。 图 3 为电解抛光前后钛镍丝材表面粗糙度,图 4 为抛光前后钛镍丝材表面形貌立体图。 抛光前钛镍丝材平均粗糙度为 161.3 nm,且波动大;抛光后粗糙度大幅度降低,波动也较小,整体较为均匀,其中抛光液 4 的抛光效果好,平均粗糙度为 15.6 nm,与图 2 结果相符。
2.3 抗腐蚀性
图 5 为抛光前后钛镍合金丝材在 37 ℃ PBS 中的极化曲线,利用塔菲尔外推法对其进行分析,得到了各样品的自腐蚀电位与自腐蚀电流,如表 3 所示。 自腐蚀电位从-0.167 V 提高至 0.045 V,自腐蚀电流密度有所降低,表明经电解抛光后,钛镍合金丝材抗腐蚀性有所提高。 钛镍合金在人体中主要发生点蚀和均匀腐蚀,前者速度远远大于后者,抛光前表面粗糙不平,划痕深度、长度不一,以孔蚀为主;抛光后表面平整、光滑,以均匀腐蚀为主,可见抛光后抗腐蚀性能有所提升。
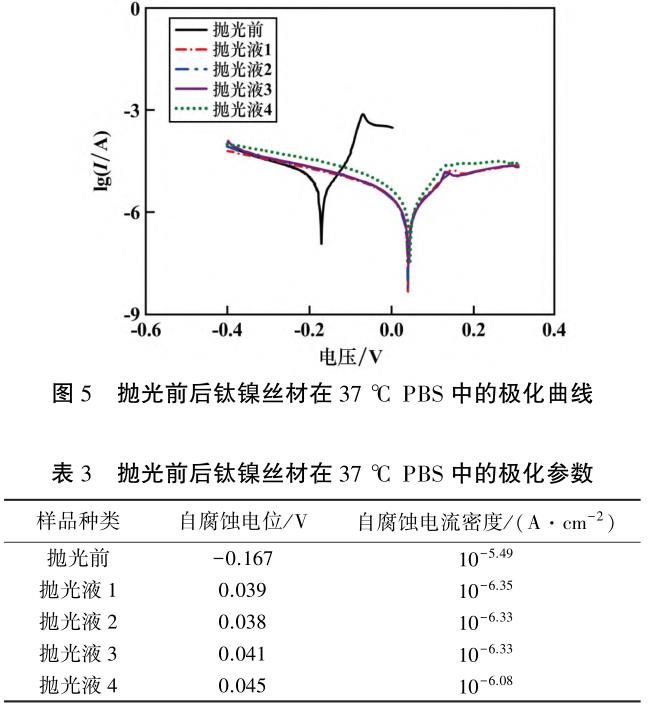
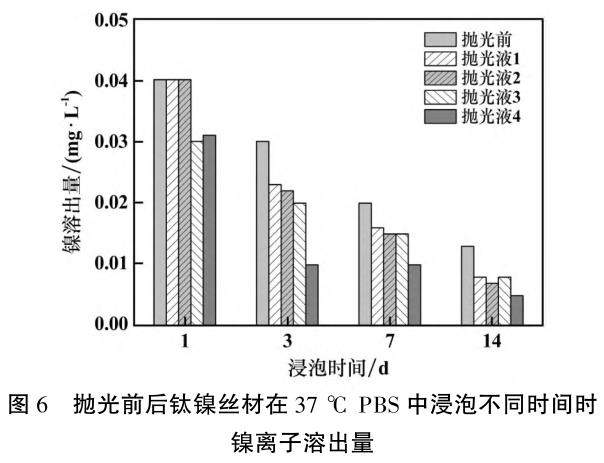
图 6 为抛光前后钛镍丝材在 37 ℃ PBS 中浸泡不同时间时镍离子溶出量。 由图 6 可知,5 组样品的镍溶出量都随着浸泡时间增加而减少。 抛光前样品的镍溶出量一直很高,与其抗腐蚀性能差相一致。 这是因为自然条件下粗糙表面形成的氧化层并不均匀,电化学不均匀区域更容易发生腐蚀,样品经初步机械抛光,近表面区域往往会展现较高水平的镍[12],腐蚀发生后镍的溶出量高。 经抛光液 4 抛光后的样品镍溶出量在第 3 d 已经下降到较低水平,这是因为抛光后样品表面平整均匀,在 PBS 中生成一层均匀致密的氧化膜,抗腐蚀性能提高,阻止了镍离子的溶出。 经抛光液 1、2、3 抛光后的样品表面质量虽然有所提高,形成了氧化膜,但依然存在部分坑蚀,镍离子可能通过坑蚀溶出,镍溶出量较抛光前样品有所降低,但依然高于经抛光液 4 抛光后的样品。
2.4 血液相容性
表 4 为抛光前后钛镍丝材表面溶血率。 抛光前样品溶血率达到 2.333%,为轻微溶血材料,经抛光液 1抛光后样品溶血率没有明显降低,但经抛光液 2、3、4抛光后样品溶血率明显下降,其中经抛光液 4 抛光后样品溶血率降至 0.333%。 医用材料对红细胞产生的破坏包括机械损伤和材料可溶性离子化学作用两方面[14],抛光前样品表面粗糙、镍离子溶出多,划痕边角尖锐,造成红细胞膜机械损伤,镍离子可通过抑制酶的活性使红细胞结构发生变化,膜的通透性增强,使膜破裂,引起溶血。 经抛光液 1 抛光后样品虽然粗糙度有明显下降,但镍离子溶出较多,抛光液 1 抛光后样品依然轻微溶血。 抛光液 2、3、4 抛光后样品表面粗糙度和镍溶出量明显降低,材料有较好的血液相容性。
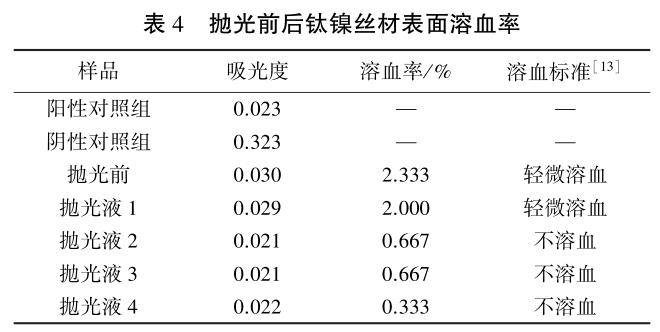
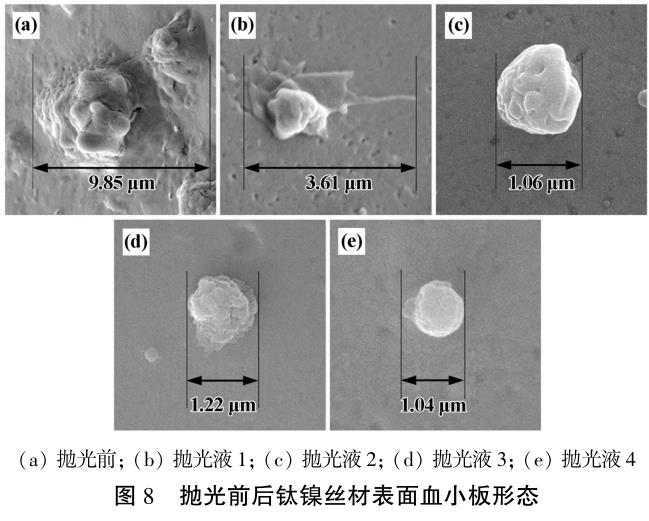
图 7 为抛光前后钛镍丝材表面的血小板黏附情况,图 8 为抛光前后钛镍丝材表面的血小板形态。 抛光前样品表面血小板聚集明显,处于激活状态。 经抛光液 1 抛光后样品表面血小板黏附多,部分血小板已经伸出伪足,血小板已经激活。 经抛光液 2、3、4 抛光后样品表面血小板黏附和聚集明显减少,血小板有轻微变形,处于初步激活。 这是因为抛光前样品表面粗糙,吸附蛋白质的有效面积增加,更容易导致血小板黏附[15]。

3、 结 论
1) 最佳抛光液组成为高氯酸⁃柠檬酸⁃甲醇⁃甘油,其中柠檬酸浓度为 2.91 g / L,甘油浓度为 83.33 mL/ L,用优化后的抛光液对钛镍合金丝材进行电解抛光,表面粗糙度由抛光前的 161.3 nm 降至 15.6 nm,表面平整光亮。
2) 抛光后样品自腐蚀电位由-0.167 V 升至0.045 V,自腐蚀电流密度由 10-5.49 A/ cm2 降至 10-6.08 A/ cm2,镍离子溶出量也明显低于抛光前样品,抛光后钛镍合金丝材抗腐蚀性能明显提高。
3) 经抛光液 4 抛光后样品溶血率由 2.333%降至0.333%,丝材表面溶血情况得到改善。 抛光前样品表面血小板聚集明显,已有铺开迹象,处于激活状态;经抛光液 4 抛光后样品表面血小板黏附数量显著减少,血小板有轻微变形,处于初步激活状态。 综合可知,抛光后钛镍合金的血液相容性得到了改善。
参考文献:
[1] 张 淼,何代华,刘新宽,等. 医用镍钛合金的电解抛光进展[ J].有色金属材料与工程, 2017,38(5):302⁃308.
[2] Simka W, Kaczmarek M, Baron W A. Electropolishing and passivaTionof NiTi shape memory alloy[J]. Electrochimica Acta, 2010,55(7):2437⁃2441.
[3] Lengyel Á, Nagy P, Bognár E. Development of NiTinol Stents: Elec⁃tropolishing Experiments[ J]. Materials Science Forum, 2012,729:436⁃441.
[4] Kim J W, Park J K, UnNithan A R. OpTimizaTion of electropolishingon NiTi alloy stents and its influence on corrosion behavior[J]. Jour⁃nal of Nanoscience and Nanotechnology, 2016,17(4):2333⁃2339.
[5] Lopes N I, Silva L Á, Santos L A. Surface characterizaTion of NiTi su⁃perelasTic and shape memory alloys after electrolyTic polishing [ J].Materials Research, 2017,20(2):572⁃579.
[6] Babilas D, Urbańczyk E, Sowa M. On the electropolishing and anodicoxidaTion of Ti⁃15Mo alloy[J]. Electrochimica Acta, 2016,205:256⁃265.
[7] 姚颖悟,王 超,赵春梅,等. 柠檬酸⁃硫酸型不锈钢电化学抛光液研究[J]. 电镀与涂饰, 2010,29(9):36⁃38.
[8] YU M, LIU J H, LI S M. Effect of electropolishing on electrochemicalbehaviours of TitaNium alloy Ti⁃10V⁃2Fe⁃3Al[ J]. Journal of WuhanUNiversity of Technology(Materials Science EdiTion), 2011,26(3):469⁃477.
[9] 李 越,李志永,柴明霞,等. 极间距和抛光液温度对镍钛合金管电解抛光的影响[J]. 电镀与涂饰, 2021,40(16):1262⁃1265.
[10]Sohei O, Takuya O, Shoichiro N. Wet etching of amorphous TiO2thin films using H3PO4⁃H2O2 aqueous soluTion[J]. Japanese Jour⁃nal of Applied Physics, 2013,52(9R):1⁃3.
[11] 杭州大学化学系分析化学教研室. 分析化学手册(第一分册)[M].北京:化学工业出版社, 1997.
[12] Trigwell S, Hayden R D, Nelson K F. Effects of surface treatment onthe surface chemistry of NiTi alloy for biomedical applicaTions[ J].Surface Interface Analysis, 1998,26(7):483⁃489.
[13] ASTM InternaTional. Standard pracTice for assessment of hemolyTicproperTies of materials: ASTM F756⁃08[ S / OL]. [ 2014⁃02⁃10].https:// www.astm.org/ f0756⁃08.html.
[14] 陈旭琼,尹庆水,张 余,等. 镁合金材料的溶血率及影响因素[J].中国组织工程研究, 2012,16(25):4632⁃4636.
[15] 张 璐,宁成云,滕 伟,等. 不同改性处理钛表面对血小板黏附行为影响的比较[J]. 中华口腔医学杂志, 2015,50(9):565⁃569.
引用本文: 彭 静,徐小宁,刘立斌. 钛镍合金丝材电解抛光工艺的研究[J]. 矿冶工程, 2023,43(6):179⁃183.
相关链接