引 言
近几十年来,金属材料由于具有良好的机械性能和生物相容性而作为植入材料被广泛应用于生物医用材料领域[1]。其中,生物医用钛合金因其适宜的弹性模量、高强度和低密度的特性在医用手术器械领域以及人工关节、骨创伤产品、心血管支架和牙齿种植体等生物医学领域有着广泛的应用[2]。例如,Ti-6A1-7Nb合金合制造用于治疗股骨颈骨骨折的中空螺钉[3],多孔镍钛合金良好的成骨性可作为人工髋关节和骨种植体[4]。但是,钛合金的一些缺点限制了其在医学生物领域的进一步应用:(1)钛合金摩擦磨损性能差,作为植入材料进入人体后可能产生的磨屑会释出 Al、V 等有害元素,引发身体炎症以及毒性反应,而作为外科辅助器材,较低的摩擦磨损性能又会降低器材的使用寿命;(2)钛合金生物活性较差,钛合金表面的惰性氧化层会降低植入体与骨组织之间的结合力,造成松动脱落而使植入失败[5-6];(3)抗疲劳性能差,钛合金表面疲劳敏感性强,造成植入物疲劳折断和塑型困难等问题;(4)抗菌性差,外部灭菌很难将细菌彻底清除极易造成其体内感染。
为提高钛合金摩擦磨损性能、抗疲劳性能、生物活性以及抗菌性能目前主要通过两种方法改善钛合金的性能,一种是通过调整合金成分来达到改善钛合金整体性能的目的。合金添加元素的细胞毒性是合金化设计需要注意的首要问题,国外学者主要选用对人体有益的钛合金β相稳定元素 Nb、Mo、Ta、Hf和中性元素Zr、Sn以及α相稳定元素 Al、O、N 等[7],但是合金化设计非常复杂且投入成本大。第二种方法是通过表面改性技术来改善钛合金性能。材料的摩擦磨损、生物活性都与材料的表面状态有关,钛合金的疲劳裂纹通常萌生在材料表面[8],对材料表面进行处理可以有效提高其耐磨性、耐疲劳性能、生物活性和抗菌性。与合金化相比,表面处理操作简单,成本更低,用表面改性技术提高钛合金性能已成为研究的热点[9]。本文就表面改性技术提高钛合金耐磨性、耐疲劳性、生物活性和抗菌性能方面的工作展开论述。
1、 表面改性提高钛合金疲劳性能
金属的疲劳断裂失效是最常见的失效形式,约占机械失效的90%[10]。钛合金常用于人体承重类植入体(如髋关节植入体),由于植入体形状不规则,在跑步、跳跃或行走等活动中处于非对称循环载荷下,疲劳失效是导致植入失败的主要原因[11]。外科用钛合金(如超声骨刀)需要在高频超声震荡下对骨组织进行切割、磨削、钻孔等,循环周次高且时间短,很容易发生疲劳使刀头断裂。在承受疲劳载荷的结构件中,疲劳裂纹会萌生于表面或内部微观缺陷处,逐渐展开会破坏疲劳寿命后期构件。通常情况,疲劳的裂纹扩展分为3个阶段:疲劳裂纹萌生、裂纹亚稳扩展和失稳扩展。如图1所示。
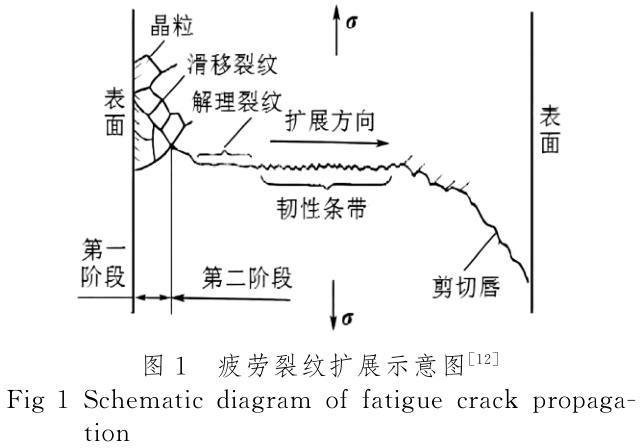
有研究表明,梯度纳米结构可以阻碍裂纹的萌生和扩展。因此在对钛合金进行表面处理时若将表面结构细化至纳米尺寸,内部保持粗晶结构,晶粒尺寸从表面到内部呈现梯度变化,可有效阻止裂纹萌生和扩展,从而提高钛合金的疲劳性能[13]。Li等[14]研究梯度纳米结构对纯钛疲劳行为的影响发现,梯度纳米结构的微观组 织 演 变 机 制 为 形 变 孪 晶、位 错 滑 移 和 相 变(HCP-FCC)的协同作用应力控制疲劳,由于显微组织和独特力学性能的协同作用,改变裂纹萌生方式,提高了钛的疲劳强度,使材料表面产生往复剧烈塑性变形的表面机械处理技术都具 有实现材料表面纳米化的潜力。

1.1 喷 丸
喷丸强化是工业上常见的表面强化方法,它通过将高速弹丸流喷射到零件表层,使表层加工硬化产生残余应力而形成一定厚度的强化层。喷丸处理后材料表面的细晶强化层和大量位错可以有效抑制疲劳裂纹的萌生,残余压应力和内部粗晶结构能够有效降低裂纹的 扩 展 速 率,从 而 提 高 裂 纹 的 疲 劳 寿 命。 Wang等[15]通过对 TC4钛合金原始试样和带有单面切口的喷丸试样进行了单轴拉伸疲劳试验,发现与未喷丸处理前的 TC4钛合金相比,喷丸处理后的 TC4 钛合金表面裂纹出现的时间比推迟了64.3%左右,疲劳寿命提高了34.2% 左 右,短 裂 纹 扩 展 速 率 降 低 约 34% ~60%。同时,罗学昆等[16]也研究了应力集中条件下喷丸对其疲劳性能的影响规律,结果显示当应力集中系数由 Kt=1(光滑试棒)提高至 Kt=2(粗糙试棒)时,TB6 试 棒 的 疲 劳 极 限 从 537.5 MPa 下 降 至335.5MPa,表现出应力 集 中 敏 感 性;而 经 过 喷 丸 后,Kt=1和 Kt=2的试棒的疲劳极限分别提高了33.5%和22.2%,缺口敏感性下降了48%。
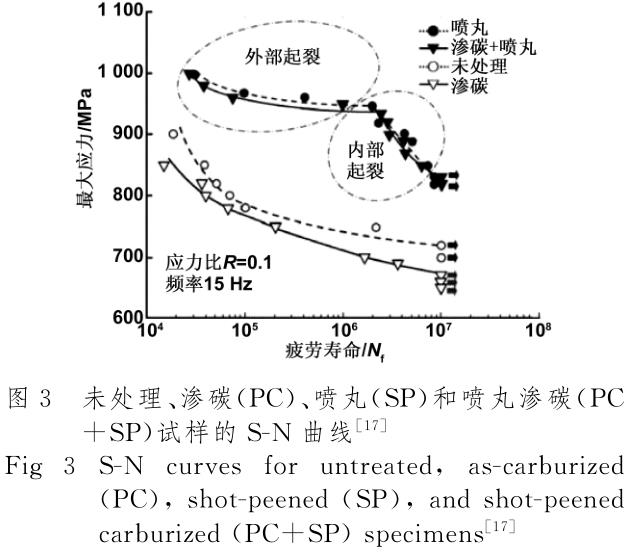
对普通喷丸技术进行改性或者与其他表面处理技术复合处理可以进一步提高钛合金的疲劳性能。Tsu-ji等[17]研 究 了 等 离 子 体 渗 碳 与 喷 丸 强 化 相 结 合 对TC4合金疲劳磨损性能的影响,发现喷丸处理可以有效改善渗碳处理 TC4合金的表面残余应力状态,使合金的 疲 劳 寿 命 提 高。研 究 发 现[18]表 面 残 余 压 应 力(CRS)随 WSP温度的升高而降低,与室温喷丸相比,温度升高提高了中低载荷下的的疲劳性寿命。刘亚鹏等[19]研究了喷丸强化(SP)和激光冲击强化(LSP)以及复合强化对 TC4疲劳性能的影响,发现激光冲击强化、喷丸强化、及其复合强化均可提高试样表面的残余压应力,但是复合强化提高得更多;相比于未强化试样,复合强化试样在疲劳应力水平提高37.9%的情况下,特征寿命提高了 57.3%。有研究结果表明[20]VF可以去除SP产生的表面损伤层,降低表面粗糙度,提高了室温下的疲劳寿命;SP+VF 处理后,TC17钛合金的室温疲劳强度提高了24.6%。经过200和300 ℃的热处理100h后,复合热处理样品的疲劳强度略有下降,但仍高于基体。罗军明等[21]也通过对比研究的方法发现喷丸+微弧氧化试样的疲劳 寿命为 13321周次,远高于微弧氧化试样的疲劳寿命3638周次,略高于原始试样疲劳寿命13067周次。综上所述,喷丸处理不仅可以提高材料的表面性能,还可以作为其他表面改性方法的预处理来改善其引入的残余拉应力和疲劳缺陷。
1.2 机械滚压
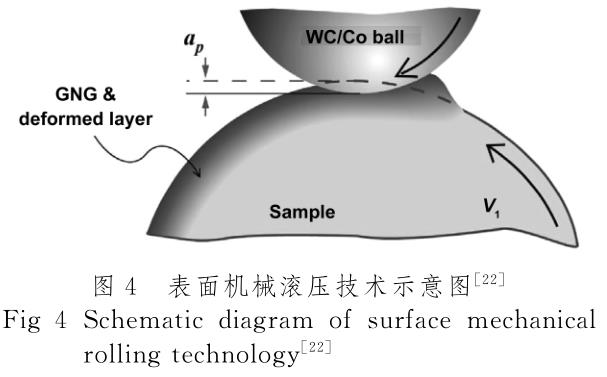
表面 机 械 滚 压 (surface mechnicalrollingtreat-ment,SMRT)技术通过硬度极高的可滚动的球体对工件表面施加一定的压力,从而使工件表面形成一层梯度纳米层[22],如图4所示。加工过程中按照预定路线对材料表面进行处理,产生的塑性流动将材料表层的波峰填入波谷,降低表面粗糙度,提高材料的表面完整性[23]。SMRT 技 术 可 以 通 过 改 变 滚 动 载 荷、滚 压 道次、滚压力等工艺参数实现对工件更加精密可控的加工[24]。利用机械滚压技术改善疲劳性能的机理可以归结为残余压应力、梯度纳米结构、表面塑性变形和表面粗糙度等因素的综合影响[25]。
有研究[26]在钛合金表面进行滚压处理后发现,钛合金的裂纹扩展门槛 值和疲劳寿命均得到明显的提高,滚压强化改善试样的疲劳性能主要是通过减缓疲劳裂纹扩展早期阶段的扩展速率实现的。2007 年天津大学提 出 表 面 超 声 滚 压 (ultrasonicsurfacerollingprocess,USRP)的 概 念,推 动 了 传 统 纳 米 技 术 的 发展[27]。USRP结合了超声频率振动和轧制的优点,在超声波冲击和静压力滚压的联合作用下,保证了滚珠和曲面的连续接触[23]。通过往复加工使表面受力均匀,产生残余应力,有效提高材料的耐疲劳性能。US-RP技术对 TC4旋转弯曲微动疲劳(FF)行为的影响,研究表明 USRP产生的残余压应力场深度为530nm,最大残余压应力为 930 MPa;经 USRP 处 理 后,TC4合金的 FF极限提高了72.7%[28]。在探究不同加工次数的 USRP技术对钛合金疲劳性能的影响中发现 US-RP处理对残余应力和疲劳性能均有所改善[29]。
2、 表面改性提高钛合金耐磨性
钛合金因表面硬度较低、摩擦磨损性能较差,并不能满足实际生产要求。对于植入物,需要具有良好的耐磨性,以免产生磨屑导致植入这身体排异反应。尤其是人造关节,往往会因为身体运动摩擦而产生微粒,这些微粒在关节组织内堆积,从而导致排异反应。对于外科用手术器械,对钛合金的耐磨性能同样有很高的要求。为解决上述问题,在钛合金表面制备耐磨涂层来提高钛合金表面的耐磨性是目前常用的方法,下面将从高硬耐磨涂层和自润滑涂层两方面来介绍耐磨涂层的研究进展。
2.1 高硬耐磨涂层
材料的硬度越高,耐磨性越好,故将材料的硬度作为材料耐磨性的重要指标之一。根据 Archard定律[30]:
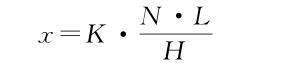
其中 K 为磨损系数,L 为滑动行程,N 为载荷,H为硬度。磨损率x 与合金的硬度成反比,提高涂层的硬度可以有效提高涂层的耐磨性。硬质涂层材料大多是过渡族金属、非金属构成的化合物和金属间化合物等。
目前,研究较多的氮化物高硬耐磨涂层主要由过渡族金属和 N 原子形成陶瓷结构的金属氮化物组成,这些强氮化形成元素的二元和三元氮化物因其键合强度高而具 有 较 高 的 熔 点、硬 度 和 耐 磨 性 等 优 良 的 性能[39](表1)。大多数过渡族金属氮化物符合 Hagg规则[40],具有 B1-NaCl结构(TiN、ZrN、CrN 等)或六方结构(NbN、TaN 等)。当前硬质氮化物耐磨涂层逐渐向成分多元化、涂层成分梯度化和纳米多层化方向发展。
成分多元化主要是在传统二元氮化物涂层的基础上添加一种或者多种其他元素来提高涂层的性能。有研究通过磁控溅射技术制备 TiAlSiN 和 TiAlN 涂层来探索摩擦性能,结果发现这两个涂层的摩擦机制相似,但 TiAlSiN 涂层的磨损率更低[41]。Soham 等[42]比较 TiN、TiAlN、TiAlSiN3种涂层的硬度发现 TiN、TiAlN 和 TiAlSiN 涂 层 的 最 大 硬 度 分 别 为 17.7,23.59,27.32GPa,添加 Al和Si后可以降低晶粒尺寸,同时提高了薄膜的弹性模量。同时 TiAlSiN 涂层中的Si3N4 相在高温下转变为 SiO2 相,导致涂层的硬度提高。
通过设计梯度涂层能够降低甚至消除涂层与基体之间的应力集中,并且降低薄膜整体的残余应力,使得基体和涂层之间的结合强度得到提高[31]。他们进一步[31]在 Ti45Nb合金表面制备了 CrN、TiAlN 单层膜和 TiAlN/CrN 多层膜并研究了其摩擦磨损性能,结果如图所示,所有陶瓷涂层都比未涂层的 Ti45Nb基体材料表现出更好的摩擦学性能,其中多层涂层样品的硬度最高,摩擦学性能最好[43]。多层涂层硬度的提高归因于周期性的界面结构,它可以阻止层间位错运动,界面位错积累对硬度的提高也有积极的作用。相似的研究结果利用 PVD 技术制备了 TiAlSiN 多层梯度涂层,TiAlSiN 多 层 梯 度 涂 层 在 常 温 下 的 摩 擦 系 数 为0.54,耐磨性能较好。耐磨性提高的原因主要是由于涂层中间的过渡层会阻断裂纹的扩展,增加抗疲劳磨损能力[44]。当调制周期在亚微米量级和微米量级之间时,多层结构可以看作是晶界对位错的钉扎效应,符合 Hall-Petch理论[45]。纳米多层化主要是通过交替沉积两种及以上纳米级厚度的结构层,在厚度方向上形成周期性交替排列的多层结构。由于纳米多层膜体系内存在大量界面,使得位错和缺陷的运动受到阻碍,从而使薄膜呈现优良的耐磨性[46]。
碳化物 涂 层 材 料 主 要 有 Ⅳ族 碳 化 物 (TiC、ZrC、HfC)、V 族 碳 化 物 (VC、NbC、TaC)和 VI族 碳 化 物(Cr3C2、MoC、WC)等。CoCrFeNiMn 高 熵 合 金 与CoCrFeNiMn-Cr3C2 复合涂层的硬度和摩擦性能的研究发现相较于 HEA 涂层,复合 HEA 涂层硬度提升40%,复合 HEA 涂层的摩擦系数为0.35,磨损量为4.9×10-4mm/(N· m)[47]。袁 明 制 备 了 NbC 涂 层,其 硬 度 为23.5GPa,磨损量为3.6×10-6 mm/(N·m),摩擦系数为0.4左右[35]。TiC涂层的性能与 TiN 的相似,都具有很高的硬度和耐磨性,但是 TiC的脆性比较大,所以通常在薄膜中加入氮元素来提高其韧性,固溶形成了单一化合物 TiC1-xNx 相[35]。TiCN 摩擦系数在0.18左右,磨损量为5×10-6 mm/(N·m),具有优异的耐磨性[48]。
金属硼化物通常是间隙相化合物,这决定了硼化物具有高硬度、化学性能稳定等特性。利用磁控溅射制备了 TiB2 涂层,其硬度为35.17GPa,磨损率为5.12×10-5 mm/(N· m)[49]。Umanskyi等[50]研 究 了Ti、Cr和Zr二硼化物的加入对复合 NiAl涂层耐磨性的影响,发现涂层的耐磨性明显高于初始金属化物涂层。添加剂的加入提高了涂层的硬度和强度,减少了金属化物基体在高温下的塑性变形,在一定程度上防止了 Ni和 Al基氧化物的破坏。
2.2 自润滑涂层
润滑剂可以减小材料接触表面的摩擦磨损,在材料表面制备一层自润滑涂层,固体润滑颗粒均匀分布在基体上,摩擦时固体润滑剂发生转移被挤入材料表面形成润滑膜,由于固体润滑剂剪切强度低,使摩擦副与材料之间形成过渡层,从而有效减小摩擦系数,减低磨损。常用固体自润滑材料的摩擦性能及特点,可以分为4类,层状固体材料(石墨、六方氮化硼(h-BN)和硫化物)、氟化物(CaF2、BaF2 等)、软金属(Ag等)和聚合物(聚四氟乙烯(PTFE))[51](表2)。
层状固体内原子呈层状排列,同层原子间作用力大,邻层原子间作用力较小,层间易剪切力和平面范德华力相对较弱,故拥有较低的摩擦系数。大气环境对石墨和硫化物的摩擦有很大影响,在潮湿环境中,石墨吸附水分和气体钝化悬垂的共价键和界面边缘以达到润滑 作 用[54],但 是 湿 度 和 氧 气 的 存 在 却 使 MoS2 和WS2 层状结构显著劣化,导致较高的摩擦系数和极短的磨损寿命[55]。针对 MoS2 对潮湿环境比较敏感的问题,耿中荣等[56]制备了 MoS2/C 复合膜并在不同湿度环境下进行摩擦实验,在低湿度环境中,MoS2 薄膜和MoS2/C 复合薄膜的摩擦性能差别不大,在高湿度环境中 MoS2/a-C 复 合 薄 膜 具 有 较 低 且 稳 定 的 摩 擦 系数,耐磨性能也明显提高。在利用双靶共溅射技术制备了 MoS2/DLC复合薄膜的研究中[57],由于加入石墨后晶粒更细,孔洞裂纹减小,韧性增强,复合膜的摩擦系数比 DLC 薄 膜 有 一 定 的 提 高,远 远 优 于 MoS2 薄膜[34]。沈玲莉等[58]发现添加 h-BN 后磨损率和摩擦系数均有所降低。
氟化物具有较低的剪切强度和稳 定 良 好 的 热 性能,此类固体润滑剂因在500 ℃时发生脆-韧转变而使涂层具备自润滑能力。有研究者采用激光熔覆法制备了含少量 CaF2(2%质量分数)的 Ni-Cr/TiB2 复合镀层发现CaF2 的加入后摩擦系数为0.24,显著提高了镀层的摩擦性能[59]。
当银、铅、锡和金等软金属作为涂层材料应用在较硬的材料表面时,由于较低的剪切应力,晶格为各向异性,晶间易滑移,产生非常低的摩擦系数(μ~0.1)[52]。
在 TiAlN 涂层中掺杂了 5 种不同含量比例的 Ag和Cu纳米颗粒后摩擦系数明显降低[60]TiAlN 涂层的主要磨损机制为磨 粒 磨 损,而 Ag-Cu 掺 杂 的 TiAlN 涂层,由于软金属颗粒的润滑作用,主要磨损机制为黏着磨损,导致复合涂层摩擦系数小。
PTFE 没有不饱和键,不易极化。在滑动接触过程中,它在接触面上形成了一层薄薄的转移膜,其接触应力较低,低分子间内聚力导致分子链容易从聚合物的结晶部分拉出,具有较低的摩擦系数[61]。PTFE 薄膜不能同时具有低摩擦系数和低磨损率,所以一般作为自润滑复合材料的基体或者添加物使用。有研究通过在 TC4表面制备 Ni-P-PTFE 自润滑复合镀层研究其磨损性能,发现添加 PTFE 后,Ni-P 的摩擦系数和磨损量都显著降低,说明嵌入的 PTFE 粒子起到了减摩和润滑作用[62]。
3 、表面改性提高钛合金生物活性
生物相容性是指医疗器械或材料在一个特定应用中引起恰当宿主反应的能力[63]。钛合金材料属于生物惰性材料,其不具备生物活性和骨诱导性,进而无法与骨界面形成良好的骨整合[63]。天然骨组织是由近致密的密质骨和多孔的松质骨组成,表面包含微米、亚微米和纳米等多级结构[64]。基于仿生学原理,钛合金表面结构尺度的差异会对钛合金生物活性产生不同的影响。研究表明具有表面粗糙、微纳米结构的植入体等有利于骨细胞的黏附、分化和增殖[65]。一方面微米级的表面结构可以提高植 入体与骨组织之间的嵌合力[66];另一方面,亚微米级的表面结构可以促进成骨细胞的生长和分化[67]。目前常用的方法主要有通过喷砂、酸蚀和碱热等工艺得到微纳多孔结构,从而提高其界面润湿性和粗糙度而提高其成骨性;表面制备生物活性涂层提高材料骨诱导性和骨结合能力。
3.1 微纳多孔结构
在植入体表面引入微纳多孔结构,可以增加材料表面的比表面积,提高粗糙度并改善界面润湿性,从而提高骨结合能力。喷砂、酸蚀和碱热复合工艺常用于微纳多孔结构的表面改进。喷砂可以去除钛表面的氧化层,使之露出新鲜的纯钛表面,且残余压应力层有利于涂层与钛表面的结合[68]。机械方法虽然在一定程度上可以改变钛表面粗糙度和表面形貌结构,但运用此方法仅能构造微米级别的粗糙表面,难以形成诱导细胞其他功能的空间尺度。在喷砂之后对钛合金表面利用不同种类或者不同浓度的酸性溶液进行酸蚀,可以去除表面的杂质,使表面光洁[69]。且行酸蚀处理后的钛表面与经过单纯机械处理的钛表面相比,具有更高的表面自由能,可以使细胞更好的与之结合,不仅促进骨整合,同时促进结缔组织与血管组织的形成与附着[68]。碱热处理法是目前制备生物活性涂层较为常用的方法之一。通过碱热法可以进一步在钛合金表面制备出微球型和纳米型形貌,并且还可以诱导形成羟基磷灰石涂层,进一步提高成骨性能[70-71]。基于多次酸蚀法在钛合金表面制备微纳米结构,Zhang等[72]发现微纳米结 构表面能促进成骨细胞粘附和增殖,并且有更好的 HA 形成能力和细胞活性。
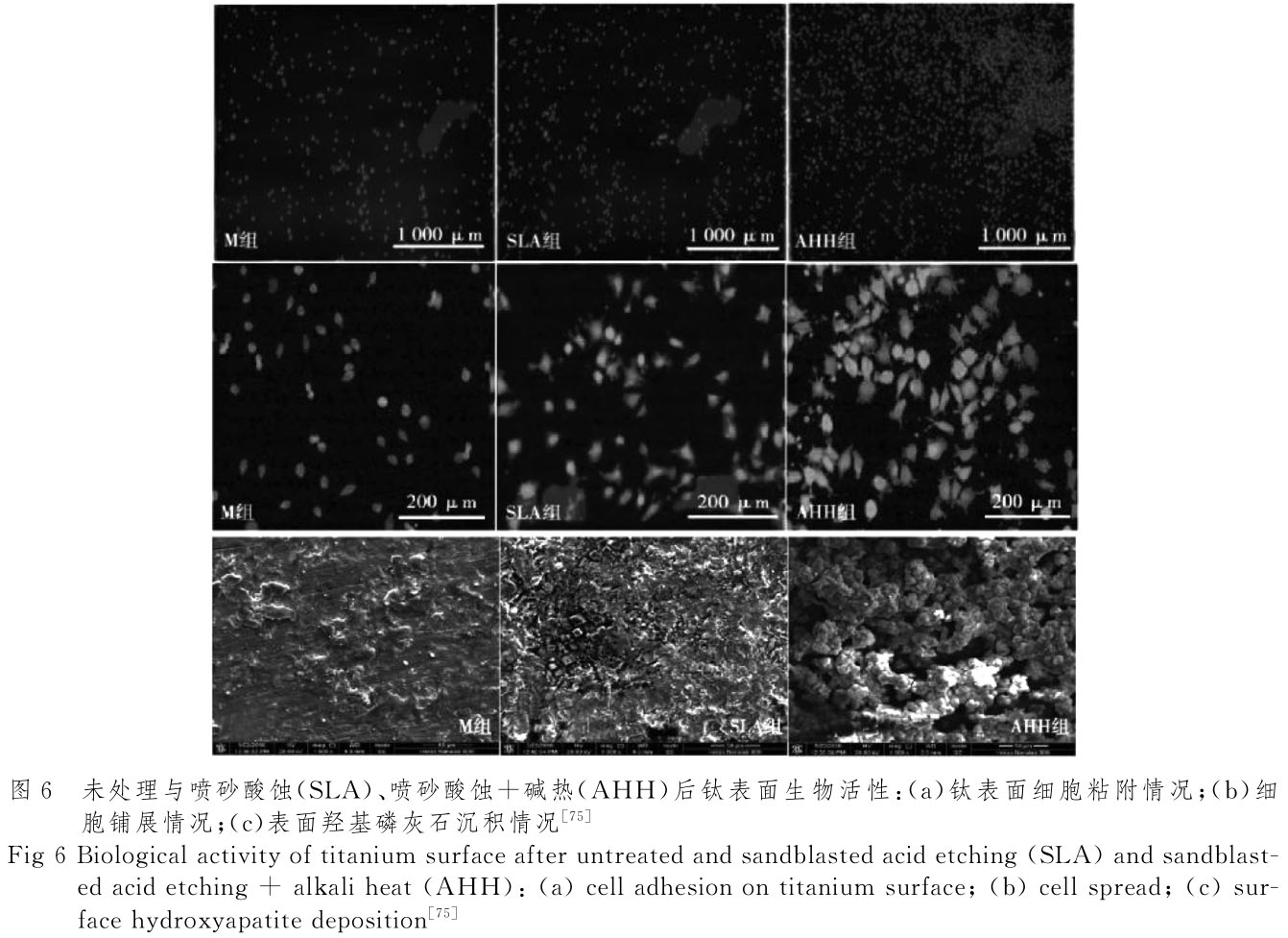
Salemi等[73]将纯钛样品碱热处理表面得到微孔表面结构,在仿生溶液放置28d后表面形成磷酸钙涂层,提高了材料的成骨性。通过对喷砂酸蚀和钛铌锆锡合金表面成骨细胞粘附、增殖和分化的影响,发现经过喷砂酸蚀处理后在材料表面 形成纳米级及微米级的凹坑,产生均匀分布的粗糙结构,经过处理后,材料仍保持亲水性;可以有效促进成骨细胞在其表面增殖、分化[74]。赵 颖 等[75]对 比 分 析 了 未 处 理 与 喷 砂 酸 蚀(SLA)、喷 砂 酸 蚀 + 碱 热 (AHH)后 钛 成 骨 性,AHH后细胞黏附、细胞铺展情况以及在模拟体液中浸泡1周后表面羟基磷灰石涂层的沉积情况都是最好的,结果如图5所示。喷砂酸蚀混合碱处理后的纯钛表面,具有更优地促进骨形成能力、表面活性和生物性能。
通过喷丸、双酸酸蚀、碱热处理的复合工艺在钛合金材料表面制备出了微纳分级多孔结构,结果表明处理后的钛合金具有良好的亲水性和 Ca/P 沉积能力,其中经过喷丸、双酸蚀 和碱热 处 理 后 界 面 润 湿 性 和 Ca/P沉积能力都达到最佳[76]。

3.2 生物活性涂层
在钛合金表面制备涂层可以在保持钛合金优异性能的同时对钛合金的表面结构、表面成分和界面润湿性等进行调整。生物活性涂层不仅可以为成骨细胞提供三维生长空间,还可以负载生物活性因子和生长因子等,促进成骨细胞的增殖分化[77]。
羟基磷灰石化学式为 Ca10(PO4)6(OH)2,是人体骨骼主要的无机成分,具有良好的生物相容性[78]。当它植入人体后,钛合金会游离出钙、磷离子而被人体吸收,新组织在骨组织表面以及 HA 涂层表面同时生长,实现骨骼和植入物之间的紧密化学键结合,并且可以充当体液与植入物之间的屏障,这样有利于植入物的稳定[79]。许莹等[80]探究 HA/MO 复合涂层的生物相容性,采 用 阳 极 氧 化 法 在 Ti-10Mo-28Nb-3Zr-6Ta合金表面先制备纳米氧化管,接着通过等离子喷涂法在纳米氧化层表面喷涂 HA 生物涂层,制备 HA/MO 纳米管复合涂层;通过细胞增殖速率分析,试样表现出优异的细胞活性,对细胞的增长速率促进效果良好。HA涂层具有多孔结构,孔隙率和孔隙直径都对成骨效果产生重要影响。就微孔孔隙率对成骨诱导能力的影响研究提示孔隙率的增加,植入物的早期骨诱导作用明显增强[81]。为了提高 HA 涂层与钛合金基体的结合率,在 TC4 表面制备了 Ti/TiN/HA 涂层,结果表明细胞外基 质 (extracellularmatrix,ECM)是 构 成细胞外微生物的主要成分,在细胞成分和周围微生物环境相互作用的过程中整合了许多细胞黏附、生存、增殖和分化等进程[83]。常用的细胞外基质蛋白有胶原蛋白、纤维连接蛋白、骨桥蛋白等。有研究在 Ti种植体表面涂覆I型胶原后发现 ECM 分子涂层可以加速骨愈合、增 加 新 骨 形 成 和 钛 骨 科 植 入 物 周 围 骨 结合[84]。Ⅰ型胶原可以通过整合素与细胞结合,将细胞外信号传递到细胞内,刺激细胞内信号通路,引导细胞附着、增殖和分化等行为。有研究发现在喷砂后的 Ti种植体表面涂覆纤维连接蛋白(FN)后,种植体的细胞黏附和细胞增殖增强[85]。等离子喷涂技术制备了多孔 HA 涂层并用胶原进行修饰,研究对比发现,间充质干细胞(MSC)在胶原修饰的 HA 涂层上的粘附、增殖和分化明显改善,部分胶原在 HA 表面的自我重建时形成纤维网络。
精氨酸-甘氨酸-天冬氨酸序列(RGD 序列)能促进成骨细胞在骨科植入物上的黏附和增殖,不仅可以刺激成骨细胞的分化,还对内皮细胞的增殖分化有积极作用[86]。田垒等[87]利用超声微弧氧化技术(MAO)在钛表面进行粗化处理后,利用多巴胺(PDA)作为偶联剂,将 环 形 肽 c(RGDfk)联 接 在 表 面,构 建 MAO-PDA-c(RGDfk)涂层,发现成骨生长肽(OGP)具有良好的骨诱导活性,当其固定在表面和支架上时可以促进成骨细胞分化和骨生长。同时也有研究发现成骨生长肽对小鼠骨髓间充质干细胞的的增殖分化,促进骨形成[88]。蒋志平等[89]在钛表面进行碱热处理后涂覆OGP涂层后发现细胞增殖情况优异,OGP 在早期可以增加 ALP活性,促进骨细胞的分化与成熟。
在骨形成和修复过程中,生长因子(骨形态发生蛋白、血小板衍生生长因子、转化生长因子等)被克隆和重组表达[90]。血小板衍生生长因子是要通过组织损伤后血小板释放,通过细胞的增殖来加快愈合。姜涛等[91]通过血管内皮细胞相关标志物鉴定,血小板衍生生长因子 BB可以促进骨髓间充质干细胞向血管内皮细胞分化。为了改善传统涂层的成骨诱导,各种生长因子(如甲状旁腺激素、骨形态发生蛋白2和成骨蛋白1)也被嵌入到多孔结构中以制造双功能植入物[92-93]。
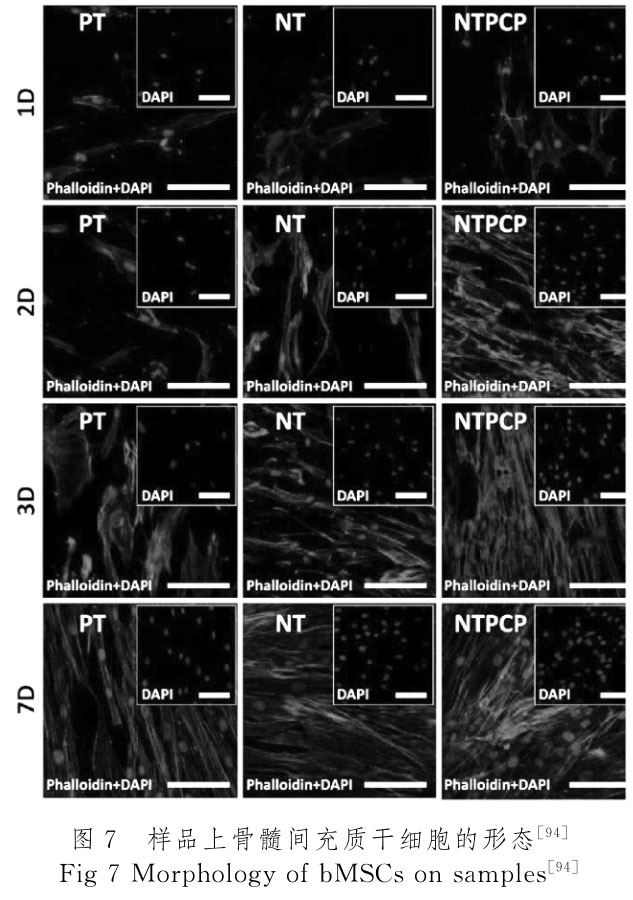
通过阳极氧化和化学介导的方式将血小板衍生生长因子固定钛表面的研究发现,生物活性/仿生表面修饰有效地增强了细胞附着、增殖、人骨髓间充质干细胞在体外的成骨行为[94]。张迪等[95]在理化修饰的基础上,引入人骨形态发生蛋白-2(hBMP-2)/人胰岛素样生长因子-1(hIGF-1),表明两种生长因子的协同能显著诱导成骨细胞的增殖、成熟与钙化。
4 、表面改性提高钛合金抗菌性
高压蒸汽等外部灭菌方法难以对细菌在医疗器械表面形成的生物膜彻底清除,从而导致临床感染。对于植入体来说,异体性以及手术操作过程都大大增加了临床感染。首先细菌细胞与材料表面之间进行快速可逆的初始相互作用,然后细菌表面结构上的蛋白质和材料表面结合分子之间 特异性和非特异性相互作用,最终形成生物膜[96],过程如图8所示。一旦形成生物膜,细菌在体内就很难被杀死。因此,防止抗菌表面形成生物膜是避免病原 体传播和材料变质的最佳途径。
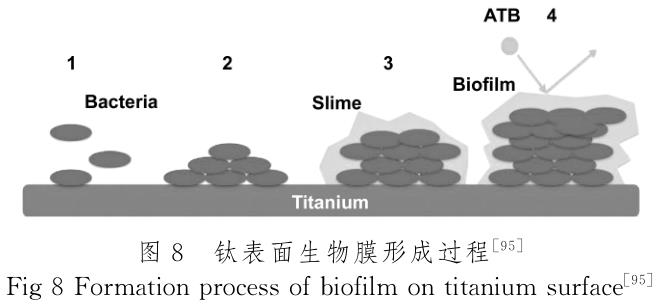
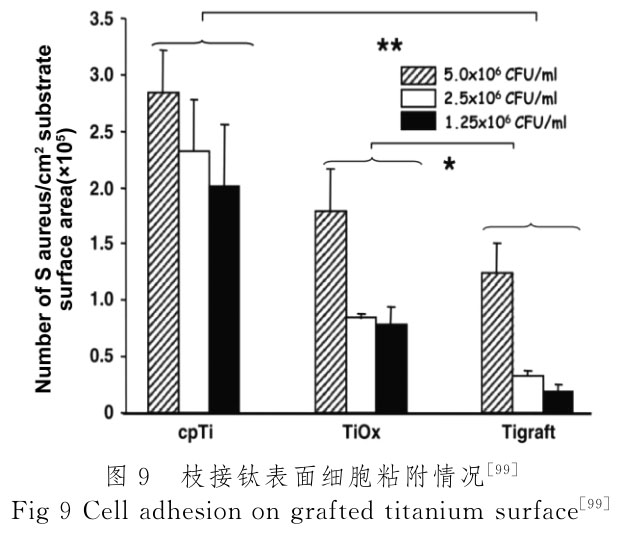
钛植入材料的表面粗糙度、化学性质、表面能和带电荷量等特性对细菌在种植体表面的初始粘附和生物膜的形成都有着重要影响[97]。因此,可以通过调节材料表面的性能来抑制细胞黏附和生物膜的形成。紫外线照射导致 Ti6Al4V 表面的自发润湿性增加,同时保持合金的体块特性,这对其作为骨科和牙科种植体的性能至关重要。在紫外线辐照后 TC4表面细胞黏附性,发现几种成骨细胞不受紫外线辐照的影响,但会导致 金 黄 色 葡 萄 球 菌 ATCC29213、表 皮 葡 萄 球 菌ATCC35984和 表 皮 葡 萄 球 菌 HAM892 的 粘 附 率 降低[98]。同时有研究通过聚苯乙烯磺酸钠(polyNaSS)以共价键枝接至纯钛(cpTi)表面对金黄色葡萄球菌黏附的影响,发现枝接钛表面金黄色葡萄球菌黏附明显减少,且并不影响成骨细胞的粘附、增殖与分化[99](图9)。
目前主要通过在材料表面涂覆抗生素、有机抗菌剂和无机抗菌剂来达到灭菌的作用。抗生素的作用机制是抑制微生物细胞壁和蛋 白 质 的 合 成、干 扰 DNA转录和翻译[100]。抗生素涂层可以在局部特定位置达到高疗效,且可以针对特定的种植部位周围的病原体,对不同种类的细菌研发了相应的抗生素涂层。有研究显示表面有依诺沙星涂层的 Ti植入体对金黄色葡萄球菌有明显抑制作用[101]。目前也有研究发现相比起纯 HA 涂 层,庆 大 霉 素-HA 涂 层 的 细 菌 感 染 显 著 降低[102]。但是抗生素的使用会产生生物耐药性,有可能对人体正常细胞造成损伤,此外,抗生素的可控长效释放也比较难以实现[103]。
无机抗菌剂在人体内成分稳定,具有良好的抗菌性能和优良的生物相容性,一般分为光催化材料和金属离子两类。光催化材料主要是通过光激发的强氧化自由基从而达到抗菌效果,如 TiO2、ZnO 和SiO2 等禁带宽度为 n型的半导体氧化物[104]。钟欣等[105]制备HA/ZnO/SiO2 涂层材料并研究其抗菌性,与 纯 HA涂层对比发现,HA/ZnO/SiO2 对于对大肠杆菌和金黄色葡萄球菌抑菌率分别为81.7%和89.4%。有研究利用溶胶-凝胶法制备 TiO2 薄膜后发现,TiO2 在自然光诱导的光催化灭活和抗细菌粘附方面表现出良好的性能[106]。常 用 抗 菌 金 属 离 子 有 Hg2+ 、Ag+ 、Pb2+ 、Cu2+ 、Zn2+ 、CO2+ 等,由于 Hg、Pb等对人体危害较大,所以 Ag、Cu、Zn等金属离子应用更加广泛[107]。金属离子抗菌机制有以下几种解释[108-109]:(1)破坏细菌细胞膜细胞壁;(2)与细胞质中的核酸和蛋白质结合从而使其失去酶的活性,影响细胞的代谢;(3)与细菌的遗传物质发生反应,导致 DNA 结构破坏而抑制细菌的增殖。基于纳米银羟基磷灰石涂层白色葡萄球菌的研究提 示,其 有 较 强 的 抑 制 作 用,抗 菌 率 均 在 95% 以上[110]。溶胶凝胶法制备的含锌碳磷灰石涂层,存在锌离子和碳酸根的取代反应,含Zn的碳磷灰石涂层材料具有良 好 抗 菌 效 果[111]。Jing 等[112]对 比 研 究 Cu 和Cu/Ag涂层的抗菌性能发现,Cu 具有较高的抗菌效果和良好的广谱抗菌性能,Ag的加入大大提高了抗菌性和抗菌谱。
有机抗菌剂可以分为天然有机抗菌剂(壳聚糖等)和合成有 机 抗 菌 剂 (季 铵 盐 类、醛 醇 化 合 物、咪 唑 类等)。有机抗菌剂通过直接接触细胞膜,使胞膜发生收缩来达到抗菌效果[113]。有机抗菌剂制备工艺较为成熟,特点是抗菌性能好,选择性强,抗菌实效快有研究通过在 TC4表面涂覆膦酸盐/季铵盐共聚物并研究其抗菌性,结果表明 TC4底物对金黄色葡萄球菌的杀菌能力从39.4%提高到98.8%,对大肠杆菌的杀菌能力从70.0%提高到99.4%[114]。
将不同种类抗菌剂结合制备复合抗菌剂也常用于钛合金植入体表面抗菌涂层。有研究在多孔氧化钛表面沉积ZnO/壳聚糖复合涂层,发现复合涂层对大肠杆菌的抑菌活性比单独的壳聚糖涂层提高了1.2倍,其原因是由于Zn2+ 离子的释放[115]。复合抗菌涂层兼顾无机抗菌剂的稳定性和有机抗菌剂的高效性,大幅度提升了抗菌涂层的适用范围。
5 、结 语
综上所述,钛合金因其低的弹性模量、高强度、低密度以及优异耐蚀性,是目前生物医学领域最常用的材料。汇总了近期通过表面改性方法对钛合金的疲劳性能、耐磨性、生物相容性和抗菌性进行提升的研究进展,探讨了目前的表面改性技术仍然存在的问题。研究结果发现,涂覆涂层存在结合力差的问题,单一的处理技术不能满足多种性能同时提升的需求,通过探索多种表面处理工艺相结合的方式提升钛合金表面质量和性能,可以在一定程度上解决单种技术存在的环境效益和经济效益等问题。不同的研究方法再次表明,未来对于医用钛合金表面改性技术的研究不能仅止于单一性能,可以根据临床的不同需求对钛合金进行相应的表面改性处理,从而提高钛合金摩擦磨损性能、抗疲劳性能、生物活性和抗菌等综合性能。
参考文献:
[1] ShadanbazS,DiasGJ.Calcium phosphatecoatingson magnesium alloysforbiomedicalapplications:areview [J].ActaBiomater,2012,81):20-30.
[2]RenJS,ZhangY M,TanJ,etal.Currentresearchsta-tusandtrendoftitanium alloysforbiomedicalapplica-tions[J].MaterialsReports,2016,30(S2):384-388(in Chinese).
任军帅,张英明,谭 江,等.生物医用钛合金材料发展现状及趋势[J].材料导报,2016,30(S2):384-388.
[3]WeiFR,Wang H,JinX D,etal.Biomedicaltitanium alloymaterialsandtheirapplications[J].WorldNonfer-rousMetals.2018(2):260-262(inChinese).
魏芬绒,王 海,金旭丹,等.生物医用钛合金材料及其应用[J].世界有色金属.2018(2):260-262.
[4]BansiddhiA,SargeantTD,StuppSI,etal.PorousNi-Tiforboneimplants:areview[J].ActaBiomaterialia,2008,4(4):773-782.
[5]ThomsenP,LarssonC,EricsonLE,etal.Structureof theinterfacebetweenrabbitcorticalboneandimplantsof gold,zirconium andtitanium[J].Journalof Materials ScienceMaterialsinMedicine,1997,8(11):653-665.
[6]Geetha M,Singh A K,AsokamaniR,etal.Tibased biomaterials,the ultimatechoicefor orthopaedicim-plants – areview[J].Progressin MaterialsScience,2009,54(3):397-425.
[7]YuZT,YuS,ChengJ,etal.Developmentandapplica-tionofnovelbiomedicaltitaniumalloymaterials[J].Acta MetallurgicaSinica,2017,53(10):1238-1264(inChi-nese).
于振涛,余 森,程 军,等.新型医用钛合金材料的研发和应用现状[J].金属学报,2017,53(10):1238-1264.
[8]HuangJ,MaJ,WuL,etal.Microstructureandwear resistanceofWS2/WcompositecoatingonTC4titanium alloysurface[J].JournalofPhysics:ConferenceSeries,2021,1885(3):032046 (6pp).
[9]YuS,YuZT,NiuJL,etal.Researchprogressofsur-face/interfaceinteractionbetweentitaniumalloyimplants andhumantissue[J].HotWorkingTechnology,2017,46(22):18-22(inChinese).
余 森,于振涛,牛金龙,等.钛合金植入物与人体组织表面/界面相互作用研究进展[J].热加工工艺,2017,46(22):18-22.
[10] CampbellFC.ElementsofMetallurgyandEngineering Alloys[M].Almere:ASMIntermational,2008.
[11] AkahoriT,Niinomi M.Fracturecharacteristicsoffa-tiguedTi-6Al-4VELIasanimplantmaterial[J].Materi-alsScience& EngineeringA,1998,243(1-2):237-243.
[12] Sun M C.Metalmechanicproperty[M].Beijing:China MachinePress,2003(inChinese).
孙茂才.金 属 力 学 性 能 [M].北 京:机 械 工 业 出 版 社,2003.
[13] LuK.Gradientnanostructuredmaterials[J].ActaMetal-lurgicaSinica,2015,51(1):1-10(inChinese).
卢 柯.梯度纳米结构材料[J].金属学报,2015,51(1):1-10.
[14] LiX,SunB H,GuanB,etal.Elucidatingtheeffectof gradientstructureonstrengthening mechanismsandfa-tiguebehaviorofpuretitanium[J].InternationalJournal ofFatigue,2021,146:106142.
[15] WangY,ZhangY,SongG,etal.Effectofshotpeening onfatiguecrackpropagationofTi6Al4V[J].Materials TodayCommunications,2020,25(7):101430.
[16] LuoXK,ZhaoCL,ZhaX H,etal.Effectofshotpee-ningonfatiguestressconcentrationsensitivityofTB6ti-tanium alloy[J].Materials Reports,2021,35(12):12114-12118(inChinese).
罗学昆,赵春玲,查小晖,等.喷丸对 TB6钛 合 金 疲 劳应力集中敏 感 性 的 影 响[J].材 料 导 报,2021,35(12):12114-12118.
[17] TsujiN,TanakaS,TakasugiT.Effectsofcombined plasma-carburizingandshot-peeningonfatigueandwear propertiesofTi-6Al-4V alloy[J].SurfaceandCoatings Technology,2009,203(10):1400-1405.
[18] SuH L,ZhangZ,SengD,etal.Warmshotpeeningon Ti-6Al-4Valloy:effectsoftemperatureonfatiguelife,residualstress,microstructureandmechanicalproperties [J].Journalof Alloysand Compounds,2021,882:160701.
[19] LiuYP,ShiZJ,ZhaoYZ,etal.Cut-offvalueofdetail fatigueratedstrengthofTC4titanium alloy withcom-poundstrengtheningtreatmentbylasershock peening andshotpeening[J].ChineseJournalofLasers,2020,47(5):371-378(inChinese).
刘亚鹏,史志俊,赵一昭,等.激光冲击与喷丸复合强化对 TC4 钛 合 金 细 节 疲 劳 额 定 强 度 截 止 值 DFR 的 影 响[J].中国激光,2020,47(5):371-378.
[20] ShiH,LiuD,PanY,etal.EffectofshotpeeningandvibrationfinishingonthefatiguebehaviorofTC17titani-umalloyatroomandhightemperature[J].International JournalofFatigue,2021,1(2):106391.
[21] LuoJM,ChenY H,HuangJ,etal.Effectofshotpee-ningand micro-arcoxidationon microstructureandfa-tiguepropertiesofTC4titanium alloy[J].TheChinese JournalofNonferrous Metals,2019,29(6):1210-1218(inChinese).
罗军明,陈 宇 海,黄 俊,等.喷 丸 处 理 和 微 弧 氧 化 对TC4合金组织 和 疲 劳 性 能 的 影 响[J].中 国 有 色 金 属 学报,2019,29(6):1210-1218.
[22] HuangJK,WangJB,LuZ,etal.Fatiguebehaviorsof AISI316Lstainlesssteelwithagradientnanostructured surfacelayer[J].ActaMaterialia,2015,87:150-160.
[23] Chen W,Wang Q,ZhaiC,etal.Microstructureand propertiesofin-situZn-Al-Sisurfacecompositesprepared bycentrifugalcasting[J].ChineseJournalofNonferrous Metals,2001,11(3):416-423.
[24] CarneiroL,Wang X,Jiang Y.Cyclicdeformationand fatiguebehaviorof316Lstainlesssteelprocessedbysur-facemechanicalrollingtreatment[J].InternationalJour-nalofFatigue,2020,134(5):105469.1-11.
[25] TangY Y,LiLB,WangC,etal.Researchstatusof USRPnanocrystallizationtechnology[J].SurfaceTech-nology,2021,50(2):160-169(inChinese).
唐洋洋,李林波,王 超,等.超声表面滚压纳米化技术研究现状[J].表面技术,2021,50(2):160-169.
[26] YuanXL.Studyonrollingsurfaceintegrityandanti-fa-tiguemechanismoftitaniumalloy[D].Dalian:DalianU-niversityofTechnology,2018(inChinese).
袁喜林.钛 合 金 滚 压 表 面 完 整 性 及 其 抗 疲 劳 机 理 研 究[D].大连:大连理工大学,2018.
[27] Liu Y,ZhaoX,WangD.Determinationoftheplastic propertiesofmaterialstreatedbyultrasonicsurfaceroll-ingprocessthroughinstrumentedindentation[J].Materi-alsScienceandEngineering:A,2014,600:21-31,
[28] LiuC,LiuD,ZhangX,etal.Effectoftheultrasonic surfacerollingprocessonthefrettingfatiguebehaviorof Ti-6Al-4Valloy[J].Materials (Basel),2017,10(7):833.
[29] LiuC,LiuD,ZhangX,etal.Ontheinfluenceofultra-sonicsurfacerollingprocessonsurfaceintegrityandfa-tigueperformanceofTi-6Al-4V alloy[J].Surfaceand CoatingsTechnology,2019,370:24-34.
[30] Wu L L.DryslidingtribologicalbehaviorofZr-based bulkmetallicglass[J].TransactionsofNonferrousMet-alsSocietyofChina,2012,22(3):585-589.
[31] OmakliO.InfluenceofCrN,TiAlN monolayersand TiAlN/CrN multilayerceramicfilmsonstructural,me-chanicalandtribologicalbehaviorofβ-typeTi45Nballoys [J].CeramicsInternational,2020,46(6):8185-8191.
[32] Kim S,Yoon H W,Moon KI,etal.Mechanicaland frictionbehaviorofsputtered Mo-Cu-(N)coatingsunder variousN2gasflowusingamulticomponentsinglealloy target[J].SurfaceandCoatingsTechnology,2021,412:127060.
[33] Chang Y Y,ChungC H.Tribologicaland mechanical propertiesof multicomponentCrVTiNbZr(N)coatings [J].Coatings,2021,11(1):41.
[34] ChengK H,LaiC H,LinSJ,etal.Structuralandme-chanicalpropertiesofmulti-element(AlCrMoTaTiZr)Nx coatingsbyreactivemagnetronsputtering[J].ThinSolid Films,2011,519(10):3185-3190.
[35] Yuan M.StudyonpropertiesofNbCcoatingsdeposited bydualcathodeplasmasputtering[D].Wuhan:Wuhan InstituteofTechnology,2018(inChinese).
袁 明.双阴极等离子溅射沉积 NbC涂层及其性能研究[D].武汉:武汉工程大学,2018.
[36] PejA,ChzA,SzA,etal.FabricationandwearbehaviorofTiCreinforcedFeCoCrAlCu-basedhighentropyalloy coatingsbylasersurfacealloying-ScienceDirect[J].Ma-terialsChemistryandPhysics,2020,255(5):123571.
[37] ZhangCC.FabricationofAl-Mg-Ti-Bcoatingsbyhighpowerpulsed magnetronsputtering (HIPIMS)atroom temperature[C] //TFC'17 Abstractsofthenational Symposium on thinfilm Technology.Hefei:Chinese VacuumSociety,2017(inChinese).
张聪聪.高功率脉冲磁控溅射法(HIPIMS)在室温条件下制备 Al-Mg-Ti-B涂层[C]// TFC'17全国薄膜技术学术研讨会论文摘要集.合肥:中国真空学会,2017.
[38] Dou Z.Frictionand wearenhancementof magnetron sputteredbilayerCr-N/TiB2thin-filmcoatings[J].Wear,2020,454-455:203344.
[39] LiW,LiuP,LiawPK.Microstructuresandproperties ofhigh-entropyalloyfilmsandcoatings:areview[J].MaterialsResearchLetters,2018,6(4):199-229.
[40] SongHJ,YanQ,LiM.Studyandapplicationprogress onthe metallichardnitridesandcarbidescoatings[J].MaterialsReports,2014,28(S2):491-493+496(inChi-nese).
宋慧瑾,鄢 强,李 玫.金属氮化物 和 碳 化 物 硬 质 涂 层的研究及应用 进 展 [J].材 料 导 报,2014,28(S2):491-493+496.
[41] SousaVFC,SilvaFJG,AlexandreR,etal.Studyof thewearbehaviorofTiAlSiN and TiAlN PVD coated toolsonmillingoperationsofpre-hardenedtoolsteel[J]. Wear,2021,476(1):203695.
[42] SdA,SgB,Rg A,etal.Acomparativeanalysisover differentpropertiesofTiN,TiAlNandTiAlSiNthinfilm coatingsgrowninnitrogengasatmosphere-ScienceDi-rect[J].MaterialsChemistryandPhysics,2020,258:123866..
[43] XuX,SuF,LiZ.Tribologicalpropertiesofnanostruc-turedTiAlN/W2N multilayercoatingproducedbyPVD [J].Wear,2019,430-431:67-75.
[44] WuY,XiaoLJ,WangB,etal.ExperimentalstudyonmechanicalandtribologicalpropertiesofTiAlSiN multi-layergradientcoating[J].ChinaCeramics,2020,56(9):26-42(inChinese).
吴 雁,肖礼军,王 冰,等.TiAlSiN 多层梯度涂层力学及摩擦 磨 损 性 能 试 验 研 究 [J].中 国 陶 瓷,2020,56(9):26-42.
[45] ZhouQ,RenY,DuY,etal.Adhesionenergyandrelat-edplasticdeformation mechanism ofCu/Runanostruc-tured multilayerfilm[J].Journalof Alloysand Com-pounds,2018,772:823-827.
[46] DuHJ,TianYJ.Hardeningmechanismfornano-multi-layerfilms[J].JournalofInorganic Materials,2006,21(4):769-775(inChinese).
杜会静,田永君.超硬纳米多层膜致硬机理研究[J].无机材料学报,2006,21(4):769-775.
[47] GuoZ,ZhangA,HanJ,etal.Microstructure,mechan-icalandtribologicalpropertiesofCoCrFeNiMnhighen-tropyalloymatrixcompositeswithadditionofCr3C2[J].TribologyInternational,2020,151:106436.
[48] XingK,LiB W.PreparationofTiCNcoatinganditsmi-crostructureandproperties[J].ElectroplatingandFin-ishing,2021,40(1):35-40(inChinese).
邢 珂,李博文.TiCN 涂层的制备及其微观结构和性能[J].电镀与涂饰,2021,40(1):35-40.
[49] WuB.Preparationandtribologicalbehavioroftitanium diboridecoatingontitaniumalloy[D].Hefei:University ofScienceandTechnologyofChina,2021(inChinese).
吴 彼.钛合金表面二硼化钛涂层制备及其摩擦学行为研究[D].合肥:中国科学技术大学,2021.
[50] UmanskyiO,Poliarus O,Ukrainets M,etal.High temperaturesliding wearof NiAl-basedcoatingsrein-forcedbyborides[J].MaterialsScience,2016,22(1).
[51] QuaziM M,FazalM A,HaseebA,etal.Areviewto thelasercladdingofself-lubricatingcompositecoatings [J].Lasersin Manufacturingand MaterialsProcessing,2016,3(2):1-33.
[52] ScharfT W,PrasadSV.Solidlubricants:areview[J].JournalofMaterialsence,2013,48(2):511-531.
[53] WangP,YeYS.Researchofsolidself-lubricatingcoat-ingsontitaniumalloybylasercladding[J].TitaniumIn-dustryProgress,2015,32(4):8-12,2016,36(4):481-487(inChinese).
王 培,叶源盛.钛合金表面激光熔覆固体自润滑涂层[J].钛工业进展,2015,32(4):8-12.
[54] SavageR H.Graphitelubrication[J].JournalofApplied Physics,1948,19(1):1-10.
[55] WuJS,LiJF,ZhangL,etal.Effectsofenvironment ondryslidingwearbehaviorofsilver-copperbasedcom-positescontainingtungsten disulfide[J].The Chinese Journalof Nonferrous Metals,2017,27(10):2202-2213.
[56] GengZR,LiX,ZhangG A,etal.Tribologicalproper-tiesof MoS2/a-Ccompositefilmsunderhigh/Low hu-midityenvironments[J].Tribology,2016,36(4):481- 487,2016,36(4):481-487(inChinese).
耿中荣,李 霞,张广安,等.MoS2/a-C 复合薄膜在高/低湿 度 环 境 下 的 摩 擦 学 性 能 研 究 [J].摩 擦 学 学 报,2016,36(4):481-487.
[57] JiangA,CaoX,WangZ,等.Frictionperformanceand corrosionresistanceof MoS2/DLCcompositefilmsde-positedbymagnetronsputtering[J].ResultsinPhysics, 2021,25(4):104278.
[58] ShenLL,LuBS,JiY Y,etal.Preparationandtribo-logicalpropertiesofself-lubricatingCr-C/h-BNcompos-itecoating[J].Electroplatingand Finishing,2021,40 (1):1-6(inChinese).
沈玲莉,陆宝山,季业益,等.Cr-C/h-BN 自润滑复合镀层的制备与摩擦学性能[J].电镀与涂饰,2021,40(1):1-6.
[59] YanH,ZhangP,YuZ,etal.Microstructureandtribo-logical properties oflaser-clad Ni-Cr/TiB2 composite coatingsoncopperwiththeadditionofCaF2[J].Surface and Coatings Technology,2012,206(19-20):4046-4053.
[60] Hernán D,Perea D,Gilberto B G.Developmentand characterizationofTiAlN (Ag,Cu)nanocompositecoat-ingsdepositedbyDC magnetronsputteringfortribologi- calapplications-ScienceDirect[J].Surfaceand Coatings Technology,2020,381:125095.
[61] BahadurS,TaborD.Thewearoffilledpolytetrafluoro-ethylene[J].Wear,1984,98:1-13.
[62]InstitutionBS.Biologicalevaluationofmedicaldevices-part1:evaluationandtestingwithinarisk management process[J].
[63] Liu W,YangD,WeiX,etal.Fabricationofpiezoelec-tricporous BaTiO3 scaffoldtorepairlargesegmental bonedefectinsheep[J].JournalofBiomaterialsApplica- tions,35(4-5):544-552.
[64] WangX,XuS,ZhouS,etal.Topologicaldesignand additivemanufacturingofporous metalsforbonescaf-foldsandorthopaedicimplants:areview[J].Biomateri- als,2016,83(6):127-141.
[65] BLZA,AS M,BPKC,etal.Theinfluenceofhier-archical hybrid micro/nano-textured titanium surface withtitaniananotubesonosteoblastfunctions-ScienceDi- rect[J].Biomaterials,2010,31(19):5072-5082.
[66] GittensR A,MclachlanT,Olivares-navarreteR,etal.Theeffectsofcombinedmicron-/submicron-scalesurface roughnessandnanoscalefeaturesoncellproliferationand differentiation[J].Biomaterials,2011,32(13):3395-3403.
[67] HuangQ,ElkhoolyTA,LiuX,etal.Effectsofhierar-chicalmicro/nano-topographiesonthemorphology,pro-liferationanddifferentiationofosteoblast-likecells[J]. ColloidsandSurfacesB:Biointerfaces,2016,145:37-45.
[68] ManganoC,VittoriaP,IezziG,etal.Boneresponseto modifiedtitaniumsurfaceimplantsinnonhumanprimates (papioursinus)andhumans:histologicalevaluation[J]. JournalofOralImplantology,2008,34(1):17.
[69] RenB,WanY,WangGS,etal.Effectsofsurfacemor-phologyandcompositionof medicaltitanium alloyson biocompatibility[J].SurfaceTechnology,2018,47(4): 160-171(inChinese).
任 冰,万 熠,王桂森,等.医用钛合金表面形貌与成分对生物相容性影响研究综述[J].表面技术,2018,47(4):160-171.
[70] WangH,ZhangX,WangH,etal.Enhancingtheosteo-genicdifferentiation and rapid osseointegration of3D printedTi6Al4Vimplantsvianano-topographicmodifica- tion[J].JournalofBiomedicalNanotechnology,2018,14(4):707-715.
[71] ChenZF,Zhu WJ,NingCY.Thestudyofbiominer-alizationonthesurfaceofpuretitanium [J].Chinese JournalofOralImplantology,2007,12(3):155-158+165(inChinese).
陈卓凡,朱文军,宁成云,等.纯钛表面酸碱处理及生物矿化的初 步 研 究 [J].中 国 口 腔 种 植 学 杂 志,2007,12(3):155-158+165.
[72] Zhang R,Wan Y,AiX,etal.Preparationof micro-nanostructureontitanium implantsandits bioactivity [J].TransactionsofNonferrousMetalsSocietyofChina, 2016,26(4):1019-1024.
[73] SalemiH,BehnamghaderA,AfsharA,etal.Biomimet-icsynthesisofcalcium phosphate materialsonalkaline-treatedtitanium[J].IEEE,2007,5853-5856.
[74] FengSR,LiuX,PanS,etal.Effectofsandblastand acidetchingonattachment,proliferation,anddifferenti-ationofosteoblastsonTi-24Nb-4Zr-7.9Sn[J].Journalof OralScience Research2017,33(9):933-937(in Chi-nese).
冯帅儒,刘 鑫,潘 爽,等.喷砂酸蚀对钛铌锆锡合金表面成骨细胞粘附,增殖和分化的影响[J].口腔医学研究,2017,33(9):933-937.
[75] ZhaoY,XieJY,LiDP,etalBioactivityofthepureti-taniumsurfacetreatedwithsandblasting-acid-alkaliheat treatment[J].Stomatology,2017,37(6):495-499(in Chinese).
赵 颖,谢佳雨,李大鹏,等.喷砂酸蚀混合碱热处理后纯钛表面生物活性的研究[J].口腔医学,2017,37(6):495-499.
[76] WuL H,JinMJ,LiuJN,etal.Firstprinciplesstudy ofLiCoO2 cathode materialforlithiumionbatteriesat differenttemperatures[J].JournalofFunctionalMateri- als2021,52(7):7024-7031+7051(inChinese).
吴丽煌,金明江,刘剑楠,等.复合工艺制备表面分级多孔的钛合金及生物相容性研究[J].功能材料,2021,52(7):7024-7031+7051.
[77] LiuGC,LiRY,LiangHJ,etal.Researchadvancein theosteointegrationofsurfacebioactivecoatingontitani-umalloys[J].ChineseJournalofTissueEngineeringRe- search,2017,21(6):969-974(inChinese).
刘贯聪,李瑞延,梁豪君,等.钛合金表面生物活性涂层及成 骨 效 果 的 研 究 与 进 展 [J].中 国 组 织 工 程 研 究,2017,21(6):969-974.
[78] ABY,B A Z A,CZE.Co-dopedhydroxyapatitesas potentialmaterialsforbiomedicalapplications [J].Mi-crochemicalJournal,2019,144:443-453.
[79] SubramaniR,ShinyjoyE,LouisK,etal.Fabricationof mineralssubstitutedporoushydroxyapaptite/poly(3,4-ethylenedioxypyrrole-co-3,4-ethylenedioxythiophene)bi- layercoatingsonsurgicalgradestainlesssteelanditsan-tibacterialandbiologicalactivitiesfororthopedicapplica-tions[J].ACS Appl MaterInterfaces,2016:12404- 12421.
[80] XuY,ZhaoST,CaiY Q,etal.Preparationandper-formanceanalysisofHA/MOnanotubecompositecoat-ingbyplasmaspraying[J].SurfaceTechnology,2020, 49(7):42-52(inChinese).
许 莹,赵思坛,蔡艳青,等.等离子喷涂制备 HA/MO纳米管复 合 涂 层 及 性 能 分 析 [J].表 面 技 术,2020,49(7):42-52.
[81] ChanO,Coathup MJ,NesbittA,etal.Theeffectsof microporosity on osteoinduction ofcalcium phosphate bonegraftsubstitutebiomaterials[J].ActaBiomateria- lia,2012,8(7):2788-2794.
[82] MohseniE,ZalnezhadE,BushroaA R,etal.Ti/TiN/HAcoatingonTi-6Al-4Vforbiomedicalapplications[J].CeramicsInternational,2015,41(10):14447-14457.
[83] LiuM Y,WangXD.Researchadvancesonbiofunction-alizationofimplantsurfaceinducedbyextracellularma-trix proteins[J].Chinese Journalof Prosthodontics, 2021,22(2):154-160(inChinese).
刘梦园,王旭东.细 胞 外 基 质 蛋 白 在 种 植 体 表 面 功 能 化改性的研 究 进 展 [J].口 腔 颌 面 修 复 学 杂 志,2021,22(2):154-160.
[84] RammeltS,IllertT,BierbaumS,etal.Coatingoftita-niumimplants withcollagen,RGD peptideandchon-droitinsulfate[J].Biomaterials,2006,27(32):5561-5571.
[85] JingH,TaoH,LuG,etal.Collagen-infiltratedporous hydroxyapatitecoatinganditsosteogenicproperties:in vitroandinvivostudy[J].JournalofBiomedicalMateri- alsResearchPartA,2012,100A(7):1706-1715.
[86] ZhangG,ZhangX,YangY,etal.Duallight-inducedin situantibacterialactivitiesofbiocompatibleTiO2/MoS2/PDA/RGDnanorodarraysontitanium[J].Biomaterials Science,2020,8(1):391-404.
[87] TianL,LiD C,LiM Q,etal.Invitroexperimental studyoftheeffectofc(RGDfK)Peptideonosteoblast adhesionandproliferation[J].ChineseJournalofStereo- logyandImageAnalysis,2016,21(4):430-435(inChi- nese).
田 垒,李德超,李慕勤,等.c(RGDfK)肽 影 响 成 骨 细胞黏附,增殖 的 体 外 实 验[J].中 国 体 视 学 与 图 像 分 析,2016,21(4):430-435.
[88] SunSS,LinJG.Effectofosteogenicgrowthpeptideon proliferationandosteogenicdifferentiationofmousebone marrow mesenchymalstemcells[J].ChineseJournalof Biologicals2020,33(9):989-994(inChinese).
孙姗姗 林景广.成骨生长肽对鼠骨髓间充质干细胞增殖及成骨分化的作用[J].中国生物制品学杂志,2020,33(9):989-994.
[89] JingZP,Gao M W,ChenP,etal.Osteogenicgrowth peptidecoatedpuretitanium regulatesproliferationand differentiationofosteoblastlikecells[J].JournalofPre- vention and Treatment for Stomatological Diseases,2010,18(3):121-124(inChinese).
蒋志平,高铭武,陈 鹏,等.成骨生长肽对纯钛表面成骨细胞样 细 胞 增 殖 和 分 化 的 影 响 [J].口 腔 疾 病 防 治,2010,18(3):121-124.
[90] GothardD,SmithEL,KanczlerJM,etal.Tissueengi-neeredboneusingselectgrowthfactors:acomprehensive reviewofanimalstudiesandclinicaltranslationstudiesin man[J].EuropeanCellsand Materials,2014,28(28):166-208.
[91] JiangT,MaL,LiZ Q,etal.Platelet-derivedgrowth factorBBinducesbonemarrow mesenchymalstemcells todifferentiateintovascularendothelialcells[J].Chinese JournalofTissueEngineeringResearch,2021,25(25):3937-3942(inChinese).
姜 涛,马 磊,李志强,等.血小板衍生生长因子 BB诱导骨髓间充质干细胞向血管内皮细胞分化[J].中国组织工程研究,2021,25(25):3937-3942.
[92] YuX,WangL,JiangX,TurcotteRE,etal.Biomimet-icCaP coatingincorporated with parathyroid hormone improvestheosseointegrationoftitanium implant[J]. JournalofMaterialsScience,2012,23(9):2177-2186.
[93] SaranN,ZhangR,TurcotteRE,etal.Osteogenicpro-tein-1 delivered by hydroxyapatite-coatedimplantsim-provesboneingrowthinextracorticalbonebridging[J]. ClinicalOrthopaedicsandRelatedResearch,2011,469:1470-1478.
[94] QmabC,NanJ,SshuangL A,etal.Functionalization ofaclusteredTiO2nanotubularsurfacewithplateletde-rivedgrowthfactor-BB covalent modification enhances osteogenicdifferentiationofbone marrow mesenchymal stemcells-ScienceDirect[J].Biomaterials,2020,230:119650.
[95] ZhangD,LuoZ,ZhuL,etal.Surfacemodificationofti-taniumimplantwithhBMP-2/hIGF-1forpromotingbio-compatibilityandosteogenesis[J].JournalofSouthern MedicalUniversity,2021,41(8):1277-1282(in Chi-nese).
张 迪,罗 震,朱安棣,等.人骨形态发生蛋白-2/人胰岛素样生长因子-1对钛种植体表面细胞的成骨效率的影响[J].南方医科大学学报,2021,41(8):1277-1282.
[96] ChouirfaH,BouloussaH,MigonneyV,etal.Reviewof titaniumsurfacemodificationtechniquesandcoatingsfor antibacterialapplications[J].ActaBiomaterialia,2018, 83:37-54.
[97] SongR.Constructionandhighthroughputstudyofgra-dientmicropatternedbiofilmonmedicaltitaniumsurface [D].Xiamen:XiamenUniversity,2017(inChinese).
宋 然.医用钛表面梯度微图案化生物膜层的构筑及其生物性能高通量研究[D].厦门:厦门大学,2017.
[98] Gallardo-MorenoA M,Pacha-OlivenzaM A,SaldañaL,etal.Invitrobiocompatibilityandbacterialadhesionof physico-chemically modified Ti6Al4V surfaceby means ofUVirradiation[J].ActaBiomaterialia,2009,5(1):181-192.
[99] AlcheikhA,Pavon-DjavidG,HelaryG,etal.PolyNaSS graftingontitaniumsurfacesenhancesosteoblastdiffer-entiationandinhibitsStaphylococcusaureusadhesion[J]. Journalof Materials Science: Materialsin Medicine,2013,24:1745-1754.
[100]SuJN.Clinicaleffectsofantibioticscombinedwithini-tialperiodontaltherapyonmoderatetoseverechronicpe-ri-[odontitiscomplicatedwithT2DM[J].ChineseJournal ofNewClinicalMedicine,2019,12(10):1113-1116(inChinese).
苏佳楠.抗生素联合牙周基础治疗中重度慢性牙周炎合并2型糖尿病的疗效观察[J].中国临 床 新 医 学,2019,12(10):1113-1116.
[101]NieBE,LongT,AoH Y,etal.Covalentimmobiliza-tionofenoxacinontotitaniumimplantsurfacesforinhibi-tingmultiplebacterialspeciesinfectionandinvivocme- thicillin-resistantstaphylococcusaureusinfectionprophy-laxis[J].Antimicrobial Agents and Chemotherapy,2016,61(1):e01766-16.
[102]AltV,Bitschnau A,OsterlingJ,etal.Theeffectsof combinedgentamicin-hydroxyapatitecoatingforcement-lessjointprosthesesonthereductionofinfectionratesin arabbitinfectionprophylaxis model[J].Biomaterials,2006,27(26):4627-4634.
[103]InceA,SchützeN,HendrichC,etal.Invitroinvestiga-tionoforthopedictitanium-coated and brushite-coated surfacesusinghumanosteoblastsinthepresenceofgen- tamycin[J].JournalofArthroplasty,2008,23(5):762-771.
[104]WangZX,ZhangK,WeiJH,etal.Thepresentsitua-tionandprospectofantibacterialmaterialsandantimicro-bialagents[J].China Rubber/Plastics Technologyand chemistry,2021,47(12):22-29(inChinese).
汪子翔,张 坤,卫金皓,等.抗菌材料及抗菌剂的研究现状及前景 展 望[J].橡 塑 技 术 与 装 备,2021,47(12):22-29.
[105]ZhongX,HuangZY,ZhaoM Y.Preparationandbioac-tivitytestinvitroofHA/ZnO/SiO2gradientcoatingma-terials[J].Chinese Journal ofInorganic Chemistry, 2020,36(11):2041-2047(inChinese).
钟 欣,黄紫洋,赵梦阳.HA/ZnO/SiO2 梯度涂层材料的制 备 及 其 体 外 抗 菌 活 性 测 试 [J].无 机 化 学 学 报,2020,36(11):2041-2047.
[106]Su W,WangS,WangX,etal.Plasmapre-treatment andTiO2coatingofPMMAfortheimprovementofanti-bacterialproperties[J].SurfaceandCoatingsTechnolo- gy,2010,205(2):465-469.
[107]GuoY.Applicationanddevelopmentofantibacterialma-terials[J].JournalofTextileScienceand Engineering,2017,34(1):206-209(inChinese).
郭 亚.抗菌材料的应用与发展[J].成都纺织高等专科学校学报,2017,34(1):206-209.
[108]WangL,HuC,ShaoL.Theantimicrobialactivityof nanoparticles:presentsituationandprospectsforthefu-ture[J].IntJNanomedicine,2017,12:1227-1249.
[109]XiaJL,WangC,LiuXX.Researchonantimicrobiala-gentsandtheir mechanismsofactions[J].Journalof CentralSouth University(Scienceand Technology) , 2004,35(1):31-38(inChinese).
[110]ZhouGJ,YangDP,LiuXF,etal.Antibacterialand mechanicalpropertiesofceramicbracketswithnano-sil-verhydroxyapatitecoating[J].ChineseJournalofTissue EngineeringResearch,2015,19(52):8423-8427(inChi-nese).
周冠军,杨大鹏,刘新芳,等.纳米银羟基磷灰石涂层正畸陶瓷托槽的抗菌与力学性能[J].中国组织工程研究,2015,19(52):8423-8427.
[111]Jiang H Z,ShiXC,LiaoY M,etal.ThePreparation andcharacterizationofsol-gelderivedzincmodifiedcar-bonatedhydroxyapatite[J]WestChinaJournalofStoma- tology,2008,26(3):241-243+247(inChinese).
江华洲,施心畅,廖运茂,等.含锌碳磷灰石的溶胶凝胶法制备及 性 能 表 征 [J].华 西 口 腔 医 学 杂 志,2008,26(3):241-243+247.
[112]JingH,YuZ,LiL.Antibacterialpropertiesandcorro-sionresistanceofCuand Ag/Cuporous materials[J].JournalofBiomedicalMaterialsResearchPartA,2010, 87A(1):33-37.
[113]LiLL.ResearchprogressofTi-implantsurfacecoatings [J].ChineseJournalofNewClinicalMedicine,2020,13(5):527-532(inChinese).
李伶俐,李 潇.钛 基 种 植 体 表 面 涂 层 的 研 究 进 展[J].中国临床新医学,2020,13(5):527-532.
[114]DongY N,LiuL,SunJ,etal.Phophonate/quaternary ammonium copolymers as high-efficiency antibacterial coatingfor metallicsubstrates[J].Journalof Materials ChemistryB,2021,9(39):8321-8329.
[115]MhlA,YhwbcdE,Cheng H,etal.HybridZnO/chi-tosanantimicrobialcoatings with enhanced mechanical andbioactivepropertiesfortitaniumimplants-ScienceDi- rect[J].CarbohydratePolymers,2021,257:117639.
相关链接